Bezpečnost a účinnost alogenních mezenchymálních stromálních buněk odvozených z tukové tkáně u pacientů s epidermolysis bullosa: klinické hodnocení fáze I/II
MSC-EB je klinické hodnocení fáze I/II, jež má za cíl vyhodnotit bezpečnost a účinnost podání léčivého přípravku na bázi mezenchymálních stromálních buněk u pacientů se vzácným vrozeným (genetickým) onemocněním epidermolysis bullosa (nemoc motýlích křídel). V první fázi studie bude léčivý přípravek podán dospělým pacientům, ve druhé fázi potom dětem s tímto onemocněním.
Léčivý přípravek byl vyvinut a je vyráběn CZECRIN GMP jednotkou ACIU MU. Jeho základ tvoří specializované buňky izolované z tukové tkáně zdravých dárců. Tyto buňky má každý člověk ve svém těle, kde slouží k opravám poškozených tkání a ovlivňují funkce imunitního systému – jsou schopny přirozeně tlumit přehnanou zánětlivou reakci, která se objevuje i v obtížně léčitelných kožních ranách. Podání mezenchymálních stromálních buněk by mohlo urychlit hojení chronických ran u pacientů s nemocí motýlích křídel.
Pacienti, kteří se studie účastní, jsou v péči hlavní zkoušející lékařky, MUDr. Jitky Vokurkové, Ph.D. a jejích kolegů a kolegyň z Kliniky popálenin a plastické chirurgie a MUDr. Hany Bučkové, Ph.D. a jejích kolegů a kolegyň z Dětského kožního oddělení/EB centra Fakultní nemocnice Brno.
Na vývoji přípravku i provádění studie se od počátku podílí také pacientská organizace DEBRA ČR, z. ú.
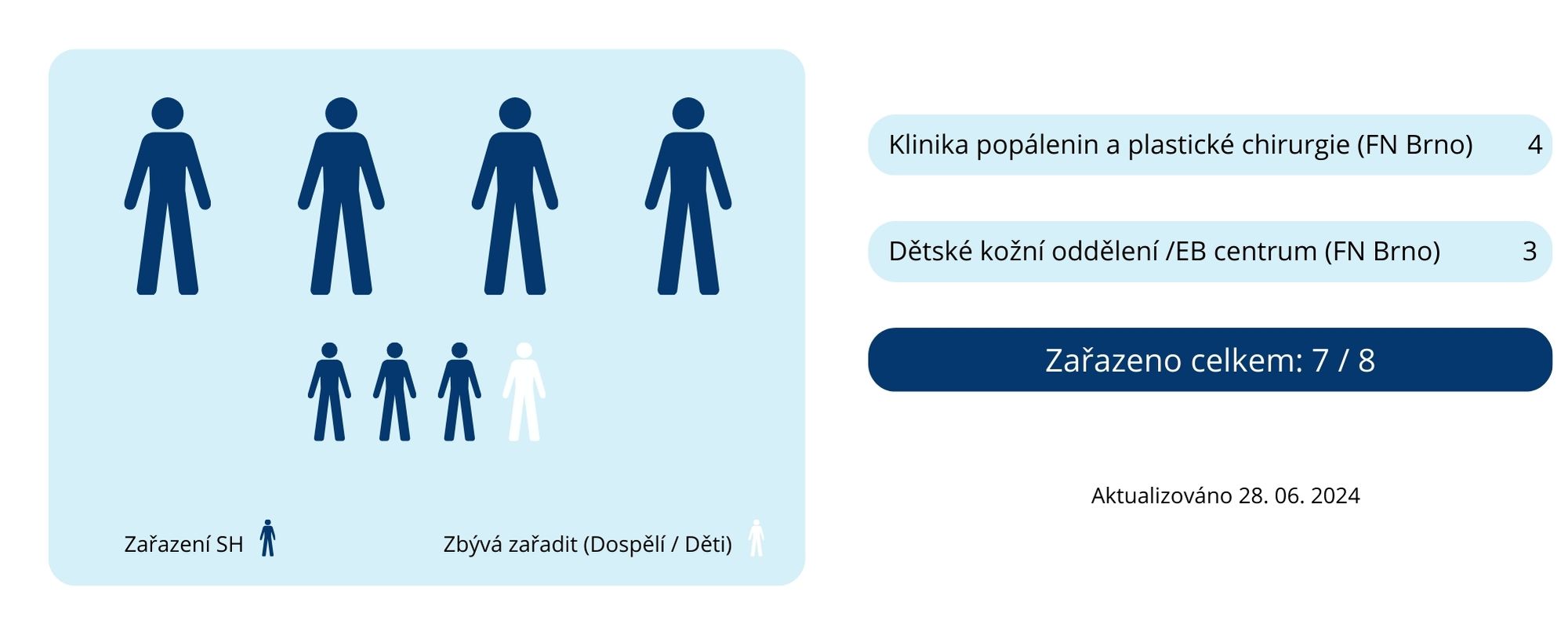
Nábor pacientů do studie byl zahájen v říjnu 2022.